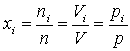 ,
,
(18-53)
Za konstantní teploty T a tlaku p ve dvousložkové směsi ideálních plynů, které na sebe chemicky nepůsobí, lze z interferogramů získaných pomocí jednovlnové interferometrie vyhodnotit koncentrace složek směsi. S takovými měřeními se lze setkat např. při výzkumu odsávání zdrojů plynných škodlivin, viz příloha P21. V této kapitole jsou uvedeny vztahy pro výpočet koncentrací směsi ve formě molárních či objemových zlomků, a to z indexu lomu ve trojrozměrném objektu a vztahy pro výpočet těchto koncentrací z interferogramů dvojrozměrných objektů - přímo z interferenčního řádu. Dále jsou zde uvedeny vztahy pro přepočet objemových zlomků na hmotnostní zlomky a vztahy pro přepočet objemových zlomků na hustoty jednotlivých složek směsi.
Pozn.: Pro současné vyhodnocení koncentrací a hustot či teplot ve dvousložkovém plynu je nutná dvouvlnová interferometrie, viz rovnice (13-3) v kap. 13.9 a v kap. 13.13.
Koncentraci i-té složky ve směsi plynů lze vyjádřit pomocí molárních či objemových zlomků
|
(18-53) |
kde ni a n jsou látková množství i-té složky a směsi, Vi a V jsou objemy i-té složky a směsi a pi a p jsou tlaky i-té složky a směsi [5-5]. Platí
|
(18-54) |
Molekulární refrakce směsi plynů N je pak dána složením směsi a molekulárními refrakcemi Ni jednotlivých složek směsi a platí [3-12]
|
(18-55) |
Výpočet objemových zlomků směsi plynů z indexu lomu
Při odvození vztahů pro výpočet koncentrací xi(x, y, z) dvousložkové směsi ideálních plynů z indexu lomu n(x, y, z), si nejdříve vyjádříme z Gladstoneova - Daleova zákona (2-14) z kap.2.9 molekulární refrakci N(x, y, z) a dostaneme
|
(18-56) |
kde M(x, y, z) je molární hmotnost směsi a r(x, y, z) je hustota směsi. Po aplikaci stavové rovnice pro ideální plyny r = p / rT a rovnice M . r = R dostaneme
|
(18-57) |
kde r(x, y, z) je plynová konstanta směsi a R je univerzální plynová konstanta. Dosazením rovnic (18-57) a (18-54) do rovnice (18-55) dostaneme pro dvousložkovou směs
|
(18-58) |
Pro koncentrace x1(x, y, z) a x2(x, y, z) jako funkce indexu lomu n(x, y, z) platí
|
(18-59) |
|
(18-60) |
Známe-li však koncentraci první složky x1(x,y,z), lze koncentraci druhé složky x2(x,y,z) vyjádřit také jednodušeji, a to pomocí vztahu x2(x,y,z) = 1 – x1(x,y,z).
Výpočet objemových zlomků směsi plynů z interferogramů dvojrozměrných objektů
V případě dvojrozměrných objektů o délce L lze vyjádřit koncentrace xi(x, y) ve dvousložkové směsi ideálních plynů přímo z rozložení změn interferenčního řádu DS(x, y). Při odvození vztahů pro výpočet koncentrací xi(x, y) vyjdeme z rovnice ideální interferometrie pro dvojrozměrné objekty (17-6) v kap. 17.4, která neuvažuje zakřivení paprsků a okrajové efekty. Z Gladstone – Daleova zákona (2-14) v kap.2.9, nebo také z rovnice (18-56) určíme indexy lomu n(x, y) a noo a po jejich dosazení do rovnice (17-6) dostaneme
|
(18-61) |
kde N(x, y) a Noo jsou molekulární refrakce směsi v místě x, y a v referenčním místě, M(x, y) a Moo jsou molární hmotnosti směsi v místě x, y a v referenčním místě, r(x, y) a roo jsou hustoty směsi v místě x, y a v referenčním místě a l je vlnová délka světla. Jelikož z Avogadrova zákona platí, že M / r = konst. [5-5], lze rovnici (18-61) upravit do tvaru
|
(18-62) |
Zavedením stavové rovnice pro ideální plyny r = p / rT a rovnice definující plynovou konstantu r = R / M , dostaneme
|
(18-63) |
Dosadíme-li do rovnice (18-63) za N(x, y) a Noo z rovnice (18-55), dostaneme vztah
|
(18-64) |
Jelikož x1(x, y) + x2(x, y) = 1, lze z rovnice (18-64) vyjádřit koncentrace x1(x, y) a x2(x, y) a můžeme psát výsledné rovnice pro výpočet koncentrací dvousložkové směsi z interferogramů dvojrozměrných transparentních objektů ve tvaru
|
(18-65) |
|
(18-66) |
Přepočet objemových zlomků na hmotnostní zlomky
Kromě molárních či objemových zlomků xi lze složení směsi definovat také pomocí hmotnostních zlomků wi. Při přepočtu objemových zlomků na hmotnostní vycházíme z definice hmotnostního zlomku a postupně dostaneme
|
(18-67) |
kde mi a m jsou hmotnosti i-té složky a směsi, Mi a M jsou molární hmotnosti i-té složky a směsi, ni a n jsou látková množství i-té složky a směsi. Molární hmotnost směsi M lze odvodit z rovnice zachování hmoty n . M = n1 . M1 + n2 . M2 + . . .
Přepočet objemových zlomků na hustoty jednotlivých složek směsi
Z objemových zlomků xi lze rovněž vypočíst hustoty jednotlivých složek ri ve směsi plynů. Zavedeme-li do stavové rovnice pro i-tou složku ve směsi definici objemového zlomku (18-53), postupně dostaneme
|
(18-68) |
kde pi a p jsou tlaky i-té složky a směsi, ri je plynová konstanta i-té složky a T je teplota směsi v daném místě.